概述
- 引起病毒性肝炎的病原体,并且是一组以肝细胞为主要靶细胞的病毒。
- 不是能引发肝炎的就称为肝炎病毒
- 肝炎病毒是指以肝细胞作为主要靶细胞,以肝脏作为主要靶器官,引发急、慢性病毒性肝炎的病毒
- 与肝脏炎症(继发性肝炎)有关的病毒
生物学形状
形态与结构
- 小RNA病毒科嗜肝病毒属;
- 形态、大小与肠道病毒相似——直径27~32nm,球形、20面体立体对称;无包膜;
- HAV电镜下呈实心颗粒和空心颗粒2种类型:
- 实心颗粒为成熟的完整病毒颗粒,具有感染性;
- 空心颗粒为缺乏病毒核酸的空心衣壳,无感染性 但具有抗原性;
- 每个壳粒由4种衣壳蛋白组成:VP1、VP2、 VP3和VP4;VP4位于衣壳内部, VP1和VP2、 VP3位于衣壳表面
- 核酸:+ssRNA——由5
末端非编码区、编码区(分为P1、P2、P3三个功能区)和3末端非编码区组成;5`末端的基因序列较保守→用于制作基因探针,核酸杂交快速诊断HAV感染;- P1区编码4种多肽VP1、VP2、VP3及VP4;其中VP1、VP2、VP3为衣壳蛋白的主要成分,含相对保守的抗原表位;但衣壳蛋白中VP4多肽含量很少或多缺如,一般检测不到,功能不清
- P2、P3区编码病毒RNA多聚酶、蛋白酶等非结构蛋白
- 7个基因型,但抗原性稳定,只有一个血清型,中和抗原决定簇位于VP1;
- 抵抗力:比肠道病毒更耐热,60℃ 1h不被灭活,100℃ 5 min、70%乙醇可使之灭活;耐酸(耐pH2-3酸性环境)、耐受乙醚、氯仿等脂溶剂;在海水、淡水、毛蚶、泥沙中存活数天至数月 。对紫外线、甲醛和氯敏感。
-
致病性与免疫性
传染源与传播途径
急性期患者和隐性感染者; 粪-口途径(粪便污染水源、食物、海产品、食具等造成散发性流行或大流行)→但发病后3周开始,粪便中不再排出病毒
- 潜伏期:15~50 d(平均30 d)
-
临床类型
临床型
- 亚临床型
-
临床特征
肝脾肿大
- 黄疸
- 转氨酶升高
- 血胆红素升高
- 恶心、呕吐、食欲减退、发热、右上腹疼痛
一般为自限性疾病,预后良好,不发展成慢性肝炎和慢性携带者。
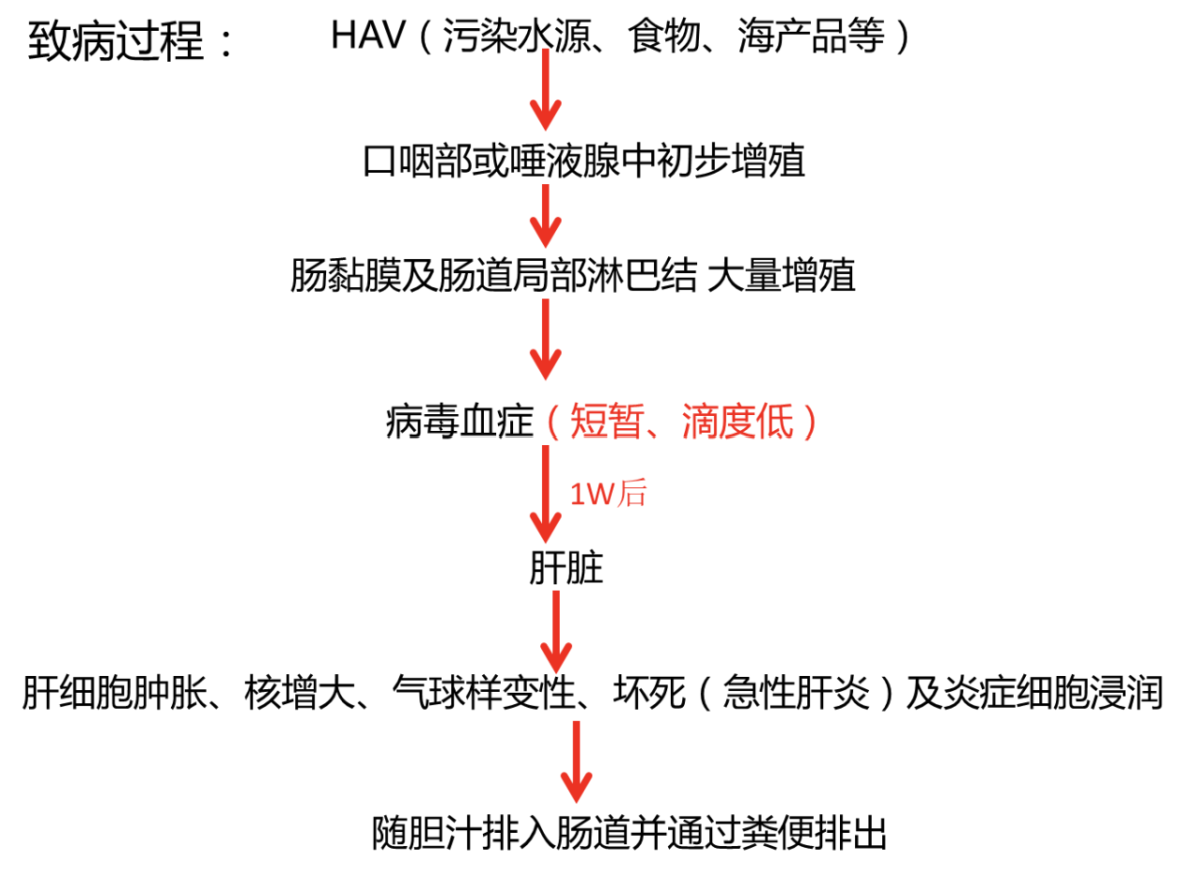
致病过程
致病机制
微生物学检查法与防治原则
- 一般不进行病原学分离检查;以测定抗原或抗体为主;亦可以RT-PCR法检测HAV-RNA
- HAV-IgM检测
- 早期、快速诊断最可靠的血清学指标
- HAV-IgG检测
- 主要用于了解既往感染史、疫苗免疫
- 效果评价或流行病学调查
- HAV-IgM检测
- 防治原则:主要通过粪便污染饮食和水源经口传染
- 预防的主要环节:加强卫生宣教工作和饮食业卫生管理,管好粪便,保护水源 丙种球蛋白→被动免疫预防作用;潜伏期→注射丙种球蛋白能预防或减轻临床症状
- 减毒甲肝活疫苗(H2株)→人胚肺二倍体细胞株连续传代减毒而制成
2008年我国将儿童接种甲型肝炎疫苗纳入国家免疫规划
乙型肝炎病毒(HBV)
Hepatitis B virus
生物学特性
形态与结构:HBV感染者的血清在电镜下可见3种不同形态的病毒颗粒:大球形颗粒、小球型颗粒和管型颗粒
- 大球形颗粒(Dane颗粒):为有感染性的HBV完整颗粒,球形,直径42nm,具双层衣壳结构。
- 小球形颗粒:中空颗粒,直径22nm,主要成分为HBsAg是病毒组装过程中过剩的外衣壳蛋白HBsAg分泌入血形成的,不含DNA和DNA多聚酶,无感染性;
- 管形颗粒:由小球形颗粒“串联” 而成。成分与小球形颗粒相似;具有与HbsAg相同的抗原性 ,不具有感染性。
小球型颗粒和管形颗粒均不是病毒体,不具有感染性;但具有与HbsAg相同的抗原性,提示乙肝病毒的感染,可能协助Dane颗粒逃避血循环中的抗-HBs综合抗体的功能
外层→外衣壳(相当于病毒包膜)
- 由脂质双层与由病毒编码的包膜蛋白组成;
- 包膜蛋白包括包括小蛋白(small protein,S蛋白)、中蛋白(middle protein,M蛋白)和大蛋白(large protein,L蛋白)
- 小蛋白:中蛋白:大蛋白=4:1:1
- S蛋白为HBsAg,M蛋白为HBsAg+ PreS2 ,L蛋白为HBsAg+ PreS2+PreS1,镶嵌于脂质双层中;
内层 →核衣壳,20面体对称(含HBcAg,dsDNA,DNA聚合酶);
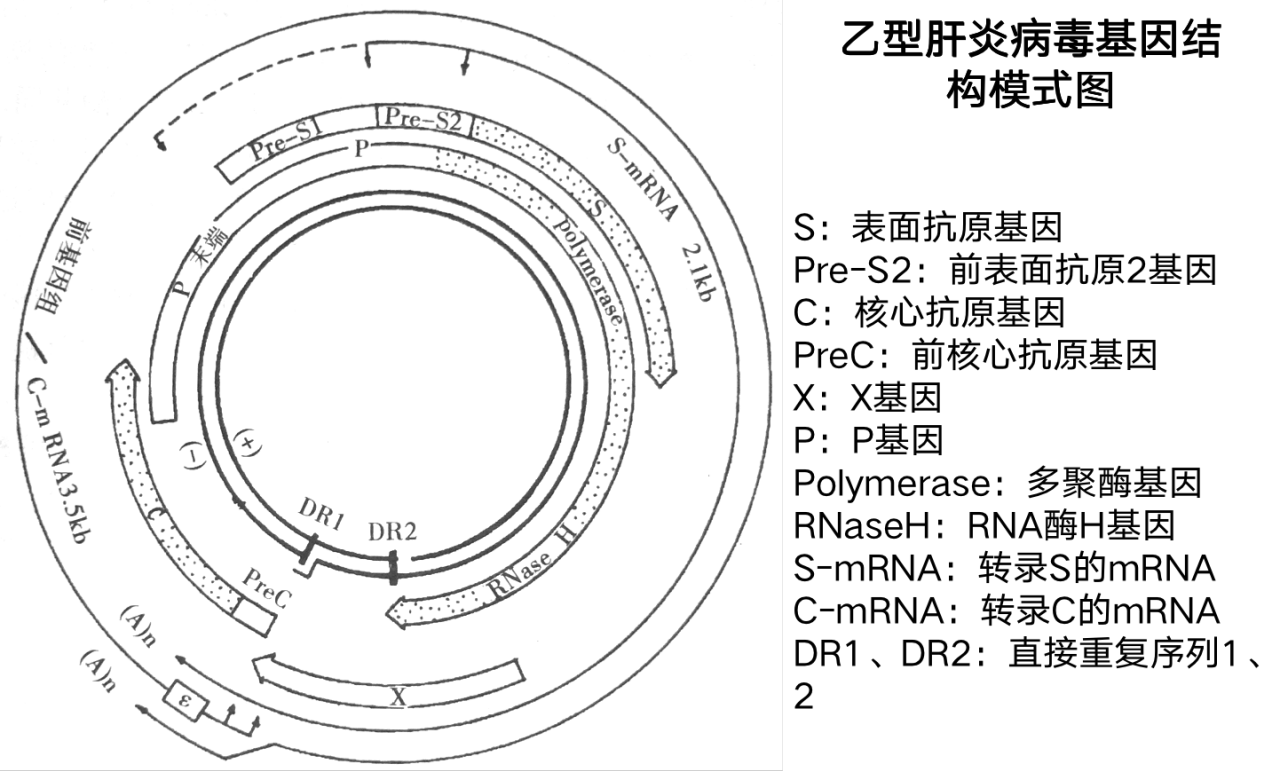
基因组为不完全双链环状DNA
- 长链(负链),具有转录模板功能;长度固定,3200 bp
- 短链(正链):只有复制功能;长度可变,为长链的50%~99%
负链含4个ORF(开放补码框): S区、C区、P区、X区,有重叠
- S区:由S基因、PreS1和PreS2基因组成
- 编码HBsAg、PreS1、PreS2
C区:含有前C和C基因
- C基因编码核心蛋白HBcAg (为衣壳蛋白)
- Pre-C与C基因共同编码Pre-C蛋白,Pre-C蛋白经切割加工后形成HBeAg,HBeAg可存在肝细胞的细胞膜表面,刺激机体产生抗HBe抗体,激活CDC(补体依赖的细胞毒作用),破坏肝细胞。血清学中HBeAg的出现通常表面病人进入恢复期。HBeAg的含量和病毒的DNA量及酶活性正相关。
- 当Pre-C基因突变时,HBeAg的出现并不一定表示病人恢复。
P区:编码DNA多聚酶(同时具有逆转酶和RNAse H活性)
- X区:编码HBxAg;X蛋白能促进HBV的复制并与肝癌的发生发展密切相关
- S区:由S基因、PreS1和PreS2基因组成
HBV复制周期
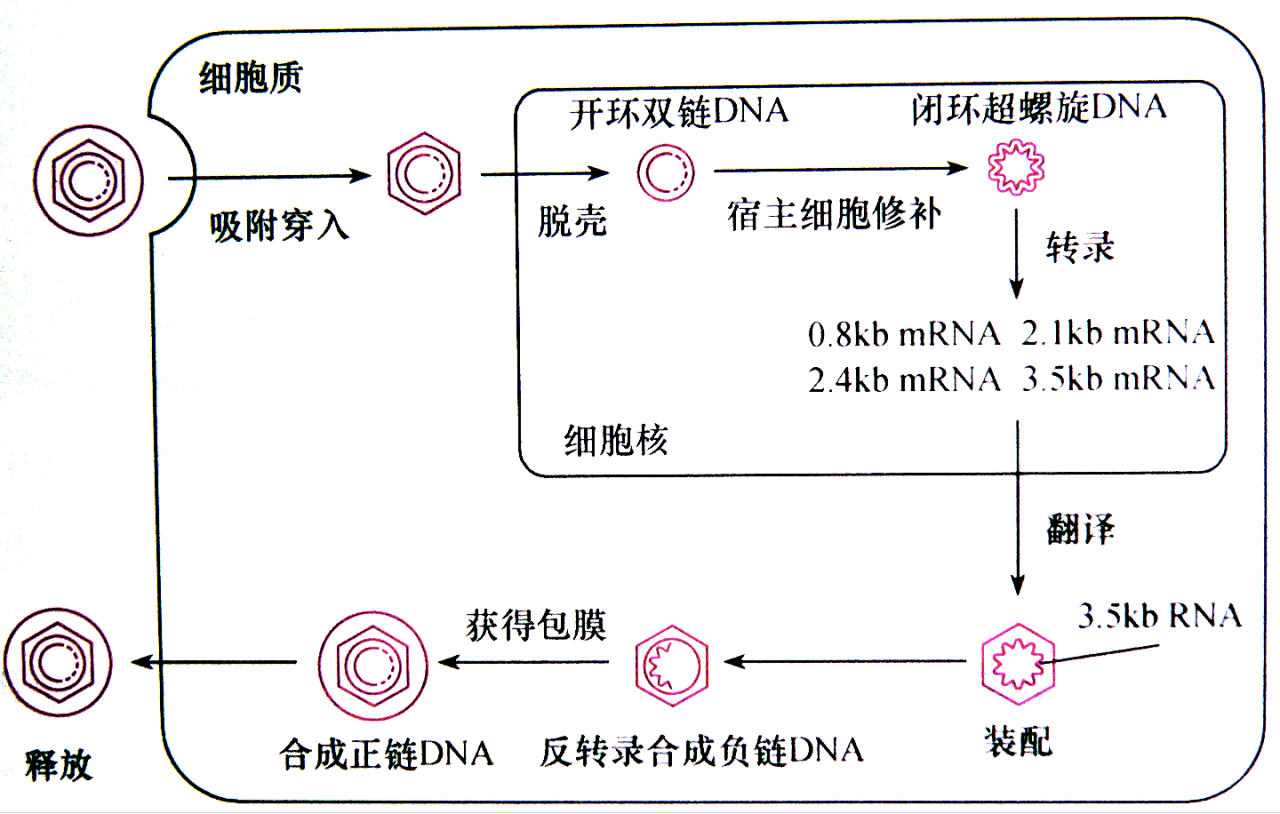
3.5kb mRNA
为二聚体蛋白→由糖基化gp27和非糖基化p24亚单位通过二硫键连接——代表HBsAg的结构单位;
- 大量存在于感染者的血液中,是HBV感染的主要标志;
- 具抗原性,刺激机体产生特异性的抗-HBs;为制备疫苗的主要成分;
- HBsAg具有四个基本亚型(a共同抗原表位,相互排斥抗原表位d/y、w/r):adr、adw、ayr、ayw,我国汉族以adr多见,少数民族以ayw多见;
PreS1及PreS2抗原: PreS1具有吸附于肝细胞受体的表位,表达高低可作为判断病毒复制的重要指标;其抗原性比HBsAg更强→抗-PreS1能通过阻断HBV与肝细胞结合而起抗病毒作用;
核心抗原(HBcAg)
存在于Dane颗粒核心结构的表面,为衣壳蛋白;
- 游离的HBcAg极少,不易在血循环中检出,不入血,故较少用于临床常规检测;
- HBcAg的抗原性强,刺激机体产生抗体,但抗-HBc为非保护性抗体;
- 抗-HBcAg IgM 绝大多数出现在第1周,多数在6个月内消失,提示HBV处于复制状态,是HBV复制的指标之一,提示急性期或慢性肝炎急性发作;抗-HBcAg IgG出现较迟,但可保持多年甚至终身,是既往感染的标记
HBcAg可在感染的肝细胞表面存在,能被杀伤性T细胞识别,在清除HBV感染细胞中有重要作用
e抗原(HBeAg)
急性HBV感染时HBeAg的出现时间略晚于HBsAg
- 由PreC及C基因编码,整体转录及转译后成为e抗原(若仅有C基因转录、转译则为HBcAg);
- 入血
- 消长与病毒体及DNA多聚酶消长基本一致→作为HBV复制及血液具有强感染性的一个指标; HBeAg的存在表示患者处于高感染低应答期
- 抗-HBe的出现是预后良好的征象,除非Pre-C基因发生突变
- HBeAg消失而抗-HBe产生称为e抗原血清转换(e antigen seroconversion );抗-Hbe阳转后,病毒多处于静止状态,传染性降低(部分患者仍有病毒复制,肝炎活动)
抗-HBe能与感染肝细胞表面的HBeAg结合→通过补体介导破坏受染的肝细胞——对HBV感染有一定的保护作用;
动物模型与细胞培养
黑猩猩对HBV最敏感。
- HBV尚不能在细胞培养中分离及培养,目前采用的细胞培养系统是病毒DNA转染系统→主要用于过筛抗HBV药物。
用S基因转染部分细胞系→可以分泌HBsAg而不含病毒其他蛋白——已用于制备疫苗。
抵抗力
HBV对外界的抵抗力较强。
- 对低温、干燥、紫外线、70%乙醇不敏感;含HBV的污染性血液在干燥环境中1周仍然具有传染性;
对高压蒸汽灭菌法、100℃加热10 min、0.5%过氧乙酸、5%次氯酸钠、0.2%苯扎溴铵和环氧乙烷敏感。
致病性与免疫性
传染源
患者或无症状HBsAg携带者(感染者的血液、尿液、唾液、乳汁、阴道分泌物、精液等多种体液中均检测到HBV)
传播途径
血液、血制品及医源性传播;
- 母-婴垂直传播:主要是围产期感染——即分娩经产道时,通过婴儿的微小伤口受母体的病毒感染;哺乳也是传播HBV的途径;部分婴 儿在母体内已被感染,表现为出生时已呈HBsAg阳性。
- 性接触传播和其它途径(公共剃刀、牙刷等)。
日常工作或生活的无血液暴露的接触,一般不会传染HBV;经吸血昆虫(蚊、臭虫等)传播未被证实
致病性与免疫机制
- 由于机体免疫功能的差异及HBV毒力的不同,致临床表现多样性(无症状带毒、急性肝炎、慢性肝炎、重症肝炎等);病毒存在于肝脏、脾脏和血细胞中;病毒增殖直接致肝细胞损害或免疫病理损害
HBV的致病机制尚未完全清楚:病毒增殖直接致肝细胞损害不是主要原因;免疫病理反应以及病毒与宿主细胞间的相互作用是肝细胞损伤的主要原因 。
免疫性
微生物血检查法
HBV血清标志物检测/HBV抗原抗体检测/两对半检查
HBsAg, HBsAb;HBeAg, HBeAb;HBcAb
- 大三阳:HBsAg(+), HBeAg (+) ,HBcAb (+)
- 小三阳:HBsAg (+), HBeAb (+), HBcAb (+)
HBsAg
- 感染早期出现, 阳性提示HBV感染并具有潜在的传染性
- 见于
- 急性乙型肝炎的潜伏期和急性期
- 慢性乙型肝炎和无症状携带者
急性肝炎恢复后1~4个月内消失 4、持续6个月以上提示为慢性肝炎或HBV携带
HBsAb
中和抗体;
- 见于恢复期、既往感染、疫苗接种后
-
PreS1、PreS2
与HBV-DNA成正比
-
PreS1-Ab、PreS2-Ab
在恢复期的早期出现(是HBV感染后最早出现的抗体)
- 阳性提示病毒正在或已经被清除
- 是预后良好的指标
-
HBcAg
不易检出
- 阳性提示病毒颗粒存在
-
HBcAb-IgM
HBV感染最早出现的抗体
- 急性HBV感染的标志物;阳性提示HBV处于复制状态;
见于急性乙型肝炎早期和慢性乙型肝炎急性发作期(急性期呈高滴度,然后下降,感 染6个月后消失);慢性乙型肝炎患者中抗HBcIgM多为阴性或低滴度
HBcAb-IgG
与抗HBcIgM几乎同时出现,但可持续终生,是感染过HBV的标志。低滴度提示既往感染,高滴度高提示急性感染;慢性乙型肝炎患者的抗HBcIgG多表现为高水平
HBeAg
与HBsAg几乎同时出现,但消失更早
- 感染的早期出现;与HBV-DNA多聚酶在血液中的动态消长基本一致
-
HBeAb
抗-Hbe阳转提示感染晚期;表示HBV病毒复制减弱、传染性降低;是HBV感染进入恢复期以及传染性减低的指标;机体获得免疫力
主动免疫与被动免疫
主动免疫
注射乙肝疫苗
第一代疫苗:HBsAg血源性疫苗(由血中提纯HBsAg并经甲醛灭活而成)——新生儿免疫3次:0、1、6个月,可获得90%以上的抗-HBs阳性率
- 第二代疫苗:基因工程疫苗——编码HBsAg的基因在酵母菌、哺乳动物细胞或牛痘苗病毒中高效率表达→纯化后获得大量HBsAg 优点:可以大量制备并排除了血源疫苗中可能存在的未知病毒的感染
第三代疫苗:HBsAg多肽疫苗或HBV DNA核酸疫苗——处于研究中
被动免疫
含高效价抗-HBs的人血清免疫球蛋白(HBIG)可用于被动免疫预防(至少100~200国际单位/ml的抗-HBs才有效果
- 紧急情况下:立即注射HBIG0.08mg/kg,7日之内均有预防效果;1个月后需再重复注射一次 ※孕妇HBsAg(+):孕28W、32W、36W分别注射一支(200μg),新生儿24小时内注射(200μg)。