联合多组学分析的好文章
胃癌是全球范围内致死率第三高的癌症类型,患者通常只有不到 40% 的五年生存率。其中约 10% 的胃癌与 EB 病毒(EBV)相关。相比于 EBV 阴性胃癌,EBV 阳性胃癌(EBV associated gastric carcinomas,EBVaGCs)具有独特的分子特征,包括 PIK3CA 高频突变,CDKN2A 表达缺失,高甲基化,以及 9p24.1 扩增等,表明 EBV 在 EBVaGCs 的肿瘤发生过程中可能扮演着重要角色。有研究提出,癌症恶化前的遗传变化与 EBV 感染有关。然而,EBVaGCs 肿瘤发生的分子时序以及介导其发展的驱动事件仍待阐述。
2021 年 9 月 8 日,北京大学生物医学前沿创新中心(BIOPIC)、北京未来基因诊断高精尖创新中心(ICG)白凡课题组与中山大学肿瘤防治中心钟茜课题组合作在Genome Medicine杂志以研究长文的形式发表题为The genomic architecture of EBV and infected gastric tissue from precursor lesions to carcinoma的论文。

该研究对来自于 25 个 EBVaGCs 患者的 123 个样本(包含了唾液,组织形态正常的胃黏膜组织,癌前病变以及肿瘤等多种类型)进行了全外显子组测序,EBV 基因组测序以及甲基化测序(图 1),从而对 EBVaGCs 发展过程中肿瘤细胞与 EB 病毒的基因组特征进行了系统的分析。
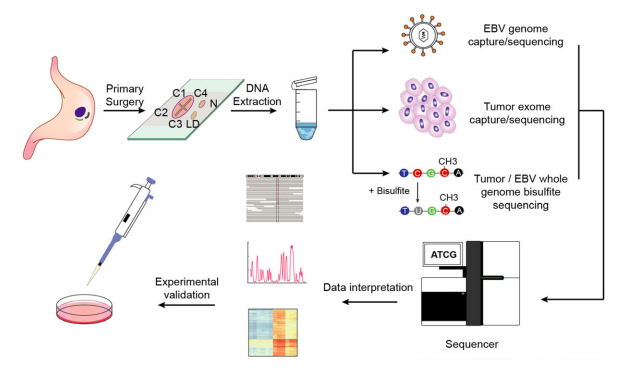
图 1. 研究方法展示
通过全外显子测序,研究者发现 EBVaGCs 和癌前病变中的重度不典型增生(high-grade dysplasia,HD)相比正常胃粘膜组织和轻度不典型增生(low-grade dysplasia,LD)具有更高的体细胞突变频率。EBVaGCs 中具有高频突变的基因主要富集在 PI3K-Akt、染色质相关通路、细胞周期调控、Wnt 和 Notch 通路,包括PIK3CA,PTEN,ARID1A,SMAD4,CTNNB1和NOTCH1等基因,其中PIK3CA和ARID1A在肿瘤中的突变频率高于其在癌前病变的突变频率(图 2)。另一方面,相比癌前病变,PI3K-Akt、RTK 和 JAK 通路相关的驱动基因拷贝数在 EBVaGCs 中明显增加;然而染色质相关信号通路或 Notch 通路相关驱动基因的拷贝数缺失事件则在癌前病变和肿瘤中具有类似的发生频率,这也表明在肿瘤发展过程中,拷贝数缺失倾向于发生在早期,而致癌基因的扩增更可能发生在后期。
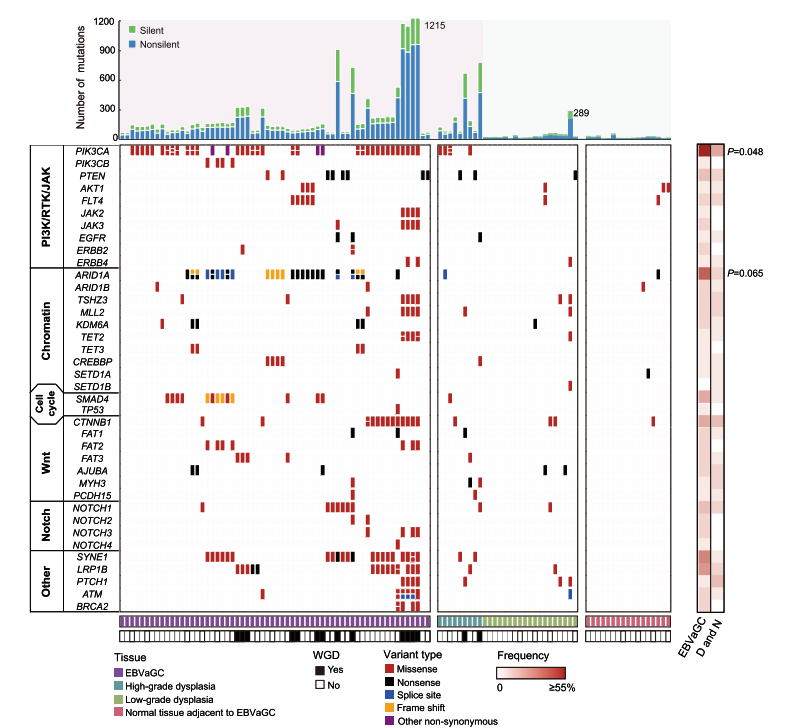
图 2. EBVaGCs 和癌前病变组织中的体细胞突变频率比较
研究者进一步对队列中每个患者的所有癌前病变与肿瘤样本进行了克隆分析,并通过构建系统发育树发现每个患者的 EBVaGCs 均为单克隆来源,并且所有 HDs 都与 EBVaGCs 具有相同的来源(图 3)。
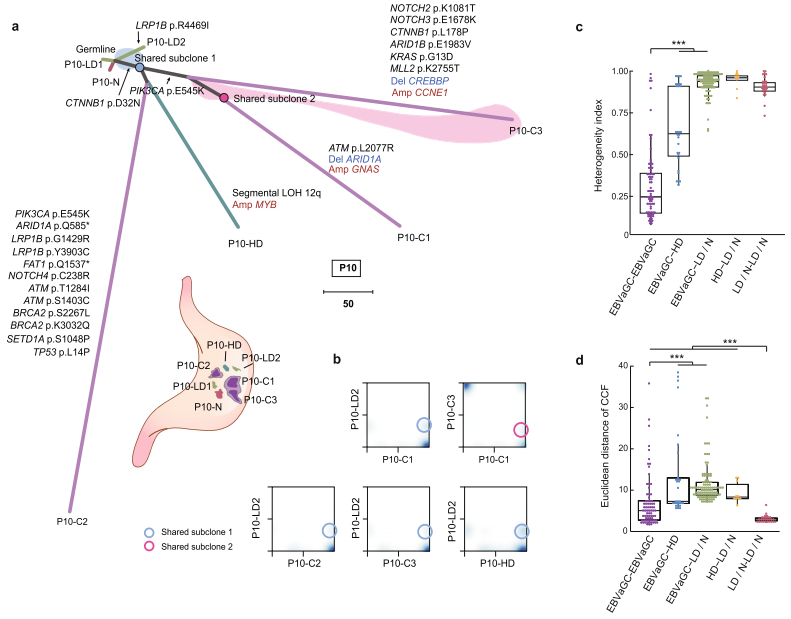
图 3. 一个典型病人的 EBVaGCs 与癌前病变组织的克隆进化关系
研究者进一步对 EBV 基因组进行了分析。首先发现了 EBVaGCs 和 HD 中 EBV 的基因组拷贝数显著高于正常胃黏膜组织和 LD,表明EBV 在癌前病变 HD 阶段即发生了大量的扩增。通过构建病毒基因组的系统发育树,研究者发现每个患者中 EBVaGCs 和 HD 的 EBV 序列高度一致,但是和正常组织以及 LD 中的 EBV 序列具有明显差异。另外,患者唾液中的 EBV 序列与 EBVaGCs 中病毒序列也明显不一致,但是和正常胃黏膜组织以及 LD 中的 EBV 序列较为相似。进一步,研究者发现正常胃黏膜组织和 LD 的 EBV 基因组相比 EBVaGCs/HD 中的 EBV 具有更高比例的杂合性单核苷酸突变(SNVs)。这可能是正常组织和 LD 存在混合毒株或者不同毒株间的重组导致的,而 EBVaGCs 和 HD 中低比例的杂合性 SNVs 则进一步证明了它们具有单株来源的 EBV。唾液,正常胃黏膜组织以及 LD,和 EBVaGCs/HD 中的 EBV 序列的多样性也暗示了在肿瘤发展过程中 EBV 毒株的受到了特异性选择。
高甲基化是 EBVaGCs 的一个显著的分子特征,有报道称 EBV 基因组中的 LMP2A 可以通过激活DNMT1和DNMT3B而导致宿主细胞基因组发生高甲基化。研究者通过全基因组甲基化测序,发现正常胃黏膜组织和 LD 的甲基化谱较为相似,但两者与 EBVaGCs 有显著差异。相对于正常组织 / LD,EBVaGCs 中存在 6316 个差异甲基化区域(DMRs),其中 99.8% 处于高甲基化状态。在所有高甲基化区域里,66.44% 与启动子区域重叠。基因通路富集分析显示这些区域包括信号转导和 Wnt 通路的负调控基因。研究人员发现,相比于癌前病变以及其他类型的胃癌,EBVaGCs 中 Ras GTPase 激活蛋白(RasGAP)家族的一些基因(包括 RASA3、RASA4、RASAL3 等)启动子区域均为高甲基化状态,提示这些基因表达沉默可能会促进 Ras 的激活从而激活下游 PI3K-Akt 通路,以进一步驱动肿瘤的发展(图 4)。为了证实这一观点,研究人员比较了胃癌细胞系 AGS 在 EBV 感染前后 RasGAP 家族基因的甲基化和表达水平,发现 EBV 感染之后 RasGAP 家族基因呈现出高甲基化、低 mRNA 水平等特征,RAS 通路活性也随之升高;而通过使用甲基化抑制剂 5-aza,则可以削弱上述效应。
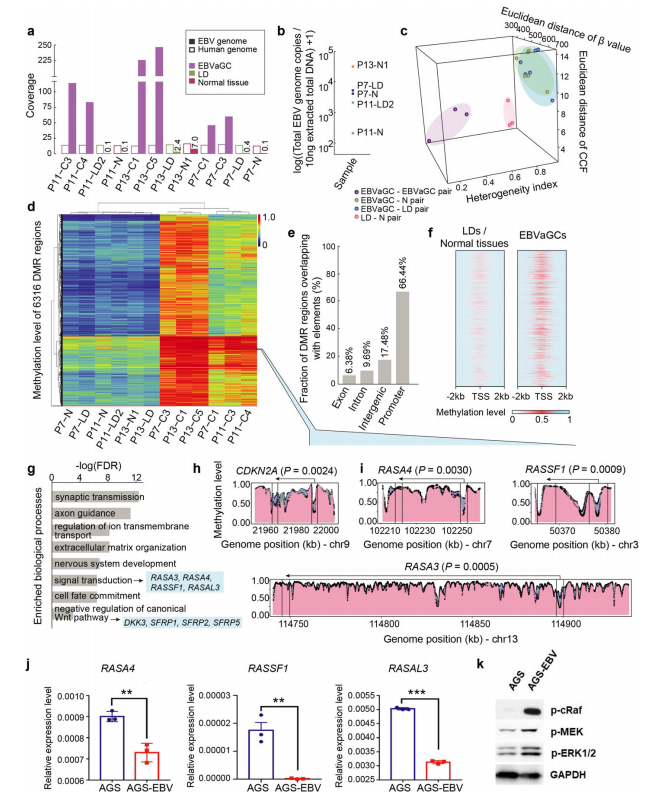
图 4. EBVaGC 与癌前病变组织中的甲基化程度对比;EBV 感染后 RasGAP 家族基因 mRNA 水平降低,RAS 通路活性升高
通过整合肿瘤发展过程中不同阶段的分子事件,研究者发现 EBVaGCs 和 HD 具有高频的 PI3K-Akt 通路基因(PIK3CA/B, PTEN),Wnt 通路基因 (CTNNB1,GNAS) 和 ARID1A 的突变以及拷贝数变异,而这些变异事件在正常胃黏膜组织和 LD 中较为罕见。结合 PI3K-AKt 和 Wnt 通路上游负调控因子启动子区域的高甲基化特征,研究者推测 PI3K-Akt 和 Wnt 通路的异常共同激活了 EBVaGCs 和 HD 中被 EBV 感染的细胞的克隆扩增,从而促进肿瘤发展。为了证明上述结论,研究者结合一系列体外和体内实验,证实 PI3K 抑制剂和 Wnt 通路抑制剂对具有 PIK3CA 和 CTNNB1 双突变的肿瘤细胞具有协同抑制作用 **(图 5)**,揭示了同时使用这两种通路的抑制剂可以作为 EBVaGCs 的一种潜在治疗策略。另外,通过研究 EBVaGCs 中宿主细胞和 EB 病毒的基因组特征和分子时序,也为针对这一特殊类型的胃癌病人进行精准治疗提供了理论依据。
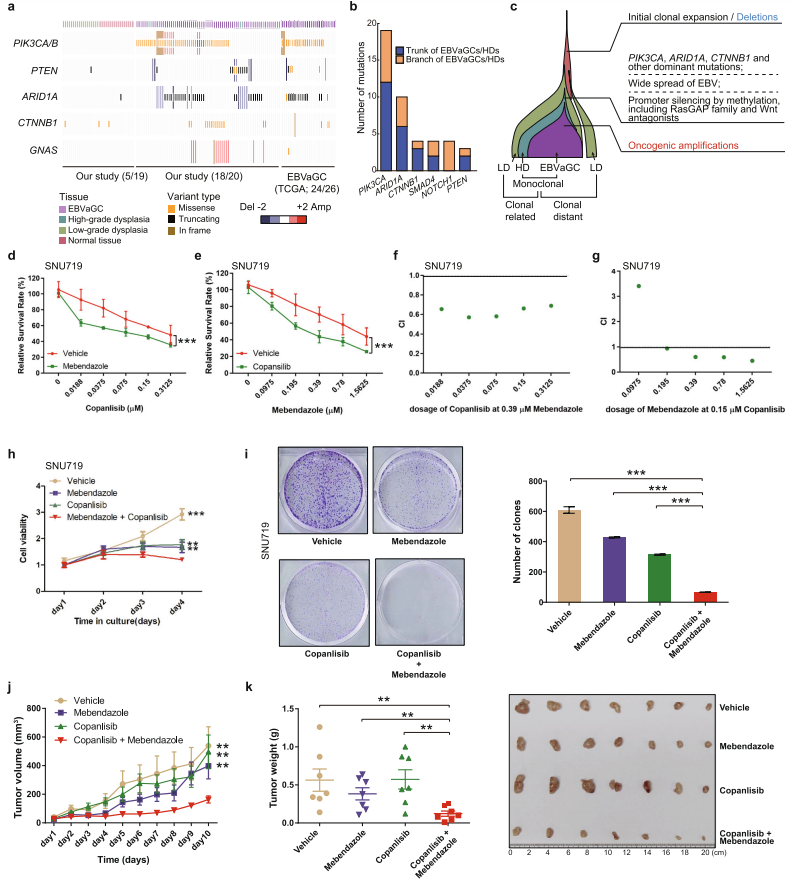
图 5. EBVaGC 驱动事件与克隆演化模型总结;细胞与小鼠实验证实 PI3K 抑制剂和 Wnt 通路抑制剂对具有PIK3CA和CTNNB1双突变的肿瘤细胞具有显著协同抑制作用
北京大学生物医学前沿创新中心陈章华博士,陈西茜博士,中山大学肿瘤防治中心颜淑梅医生、张琦医生、刘尚鑫博士研究生为本文的并列第一作者。北京大学BIOPIC 白凡研究员,中山大学肿瘤防治中心钟茜研究员为该研究论文的共同通讯作者。中山大学肿瘤防治中心曾木圣教授为本研究提供了重要指导。
原文链接:
https://genomemedicine.biomedcentral.com/articles/10.1186/s13073-021-00963-2
制版人:十一
转载须知
【非原创文章】本文著作权归文章作者所有,欢迎个人转发分享,未经允许禁止转载,作者拥有所有法定权利,违者必究。


