药物相关受体相互作用的定量测量,即受体占有率(RO),对于临床剂量确定和疗效评估已变得越来越重要。
以前有站友经常问及RO的相关问题,在此将北京生命科学研究院蛋白质组学国家重点实验室的Fu J等人在2019年Bioanalysis发表的文章里面相关内容做一下简要概述,与大家分享。
在药物开发过程中,“精密医学”概念的应用需要整合众多数据,包括药物动力学、药代动力学和安全性,以促进有关目标选择和目标验证的决策。因此,RO的定量是药物开发,尤其是细胞靶向生物治疗药物的关键药效学指标。众所周知,RO分析可帮助确定生物治疗药物的最低生物学效应水平,从而防止不良反应,包括细胞因子风暴,并建立最佳剂量方案。 RO的长期饱和可能表明药物结合过度或时间延长,可能会导致严重的副作用或毒性。
PD-1是CD28家族蛋白,免疫相关的负性调节因子之一。 PD-L1通过与肿瘤浸润淋巴细胞(TILs)表面上的PD-1分子结合来激活PD-1/PD-L1途径,从而使T和B淋巴细胞失活,并使肿瘤细胞免疫逃逸。 包括抗PD-1抗体在内的免疫治疗剂可以抑制PD-1 / PD-L1途径,从而逆转T和B淋巴细胞的失活并增强抗肿瘤免疫活性,从而达到免疫治疗效果。
在“生物标志物驱动”的临床试验中,传统的“一刀切”战略不能适用。为了消除个体差异,免疫调节剂的临床试验通常包括大约1000名受试者,RO是临床试验中的关键指标。由于RO具有多参数分析功能,因此经常使用流式细胞仪(FC)来确定RO。
中,用活化的CD45RA-CD3 +T细胞(CD45RA-CD8 + T细胞,CD45RA-CD8- T细胞)作为标记物,优化了T细胞活化标记,并开发并验证了一种用于进行抗PD-1生物治疗剂RO测量的稳健方法,可用于临床研究。除药代动力学和抗药物抗体(ADA)测量外,该研究还提供了针对PD-1抗体的RO生物分析策略的综合探索。生物分析结果的整合使你能够在剂量选择、抗癌治疗的临床疗效和安全性评估方面全面了解抗PD-1生物疗法的药理学知识。
作者这项临床试验是得到人IgG4抗PD-1抗体(JS001)进行RO分析,方法流程我整理之后,绘制如下:
计算公式则为PD−1 RO bound strategy(%)=(MFI RO Tube/MFI TR Tube)×100
部分结果: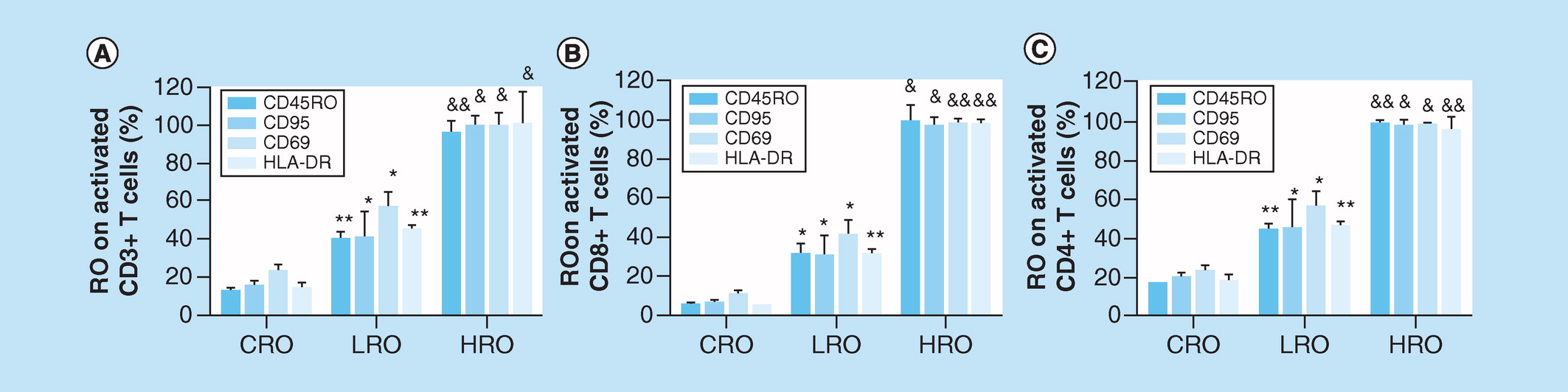
在体外向全血样品中加入不同浓度的JS001,以模拟RO状态。 选择了四个活化的生物标记以反映活化的CD3 +(A)、CD8 +(B)和CD4 +(C)T细胞中的RO表现。 根据等式1计算RO。Y轴代表在指定细胞群上被JS001占据的受体的百分比。 数据显示为平均百分率±标准差,分别由六个QC在CRO,LRO和HRO水平下计算得出。
**相对于相应的对照受体占有率(CRO)和相对应的低受体占有率(LRO),p <0.01。
CRO:基线空白; LRO:血样与JS001孵育(终浓度:0.59 pmol / l); HRO:血样与JS001孵育(终浓度:37.87 pmol / l)。
如果大家在做其它的RO试验,可以参考这篇文章试试。
信源:Fu J, Wang F, Dong LH, et al. Receptor occupancy measurement of anti-PD-1 antibody drugs in support of clinical trials. Bioanalysis. 2019;11(14):1347‐1358. doi:10.4155/bio-2019-0090

