慢性淋巴细胞性白血病(CLL)的特征是恶性B细胞克隆,临床病程缓慢。尽管取得了令人鼓舞的治疗进展,CLL仍被认为是无法治愈的疾病。CLL的预后指标有很多,例如IGHV突变状态、ZAP-70、CD38和𝛽2-微球蛋白以及某些细胞遗传学异常(例如,del17p),最近的研究提出了新的预后评分(CLL-IPI)和新的遗传标记(例如,NOTCH1和TP53突变)。
免疫化学疗法多年来一直是CLL的标准一线治疗方法,但针对B细胞受体(BCR)信号的新疗法(如ibrutinib和idelalisib)起着越来越重要的作用。沿着这些思路,最近的一些研究集中在改变BCR介导的信号转导。Le Roy等证明BCR的体外刺激会导致钙离子内流,引起活化T细胞核因子(NFAT)的表达,并可能表明NFAT2的DNA结合能力与临床结果相关。另一项研究表明表面IgM表达和细胞内钙动员依赖于IGHV突变状态和DNA甲基化。此外,多个实验室还对BCR无能状态和钙离子动员受损的特征进行了描述,认为这是惰性CLL的表现,其结局良好。
但是,既往的研究分析钙内流要么只用PBMC而没有圈中CLL细胞,要么花很多时间去分离CLL细胞。
Jonas S. Heitmann等人在4月17日J Leukoc Biol.上的文章,给我们带来了一个简单而快速反映BCR功能的钙内流检测方法。
CLL细胞先在30度用250ul含5%胎牛血清、10 µg/ml FuraRed染料的培养基培养25分钟,然后加250ul含10%胎牛血清的培养基,37度培养10分钟,接着加入1ml不含钙离子的Krebs-Ringer液洗涤离心后,接着与CD19、CD5抗体孵育20分钟,再加入20ul 4mM Ca2+的Krebs-Ringer液,此时先获取钙离子基础水平60秒,接着加入20ug/ml αIgM刺激,获取4分钟数据,最后再加入用1uM离子霉素作为阳性对照。
分析的时候,计算FuraRed的结合和未结合信号的比例。
下图是一个分析示例,先用CD5和CD19,圈双阳性信号,接着,分析此类细胞的钙离子水平随时间变化图,最后可绘制出FuraRed的结合和未结合信号比例=钙离子内流。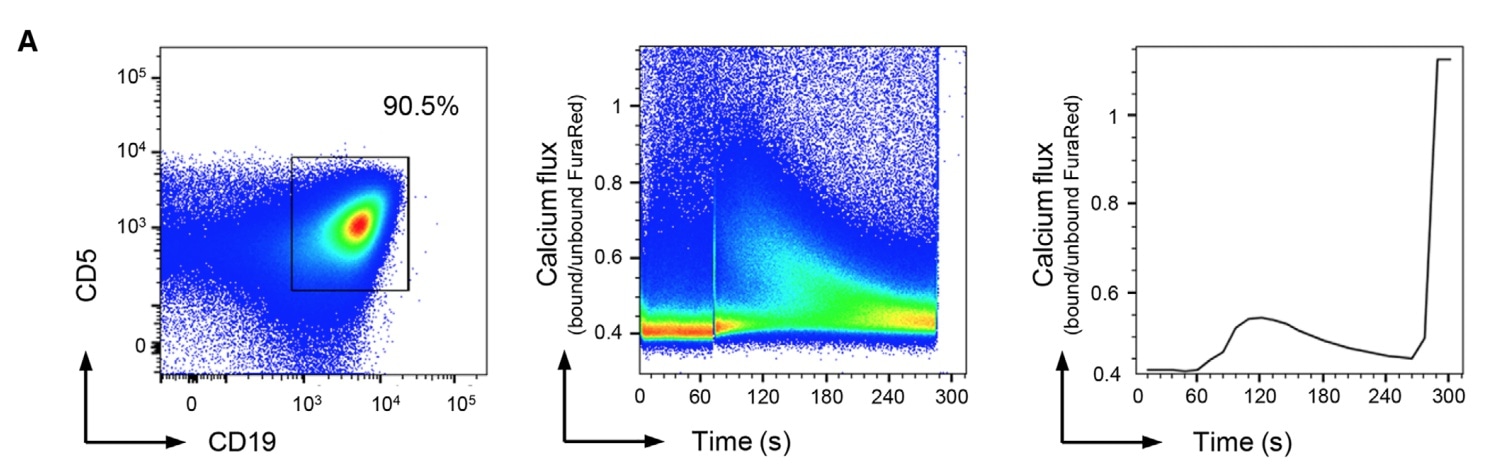
下面是4例CLL患者结果(黑、绿、红、蓝)和正常B细胞(土黄色),可见CLL患者的BCR受体总体上是受损的,但不同患者的钙离子内流水平还是有不同的: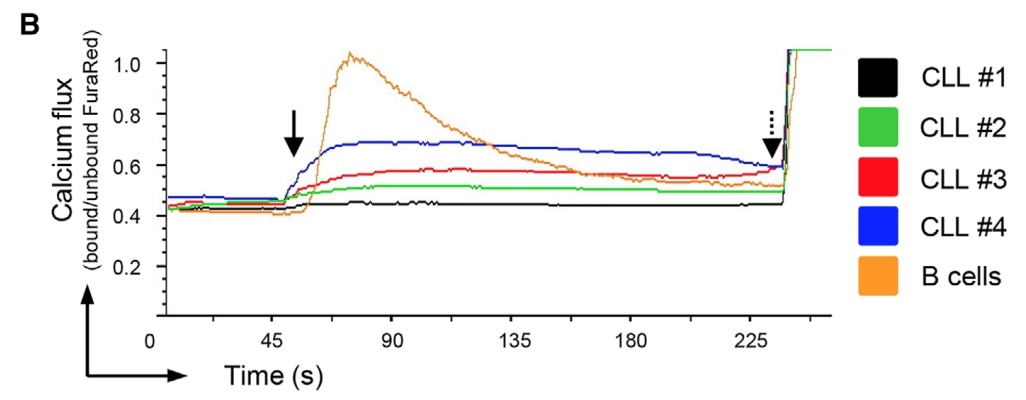
正常B细胞的钙内流水平明显比CLL患者高: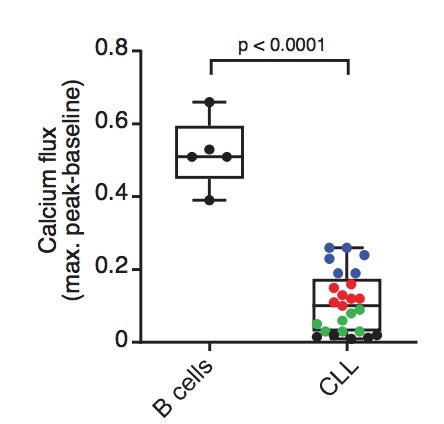
但是,即使CLL患者的钙内流受损,但其钙流水平还是可以分成四等分,最高的为蓝色、中间依次为红色、绿色、黑色,其中IGHV未突变患者的钙流水平普遍偏高,而突变患者钙流水平偏低: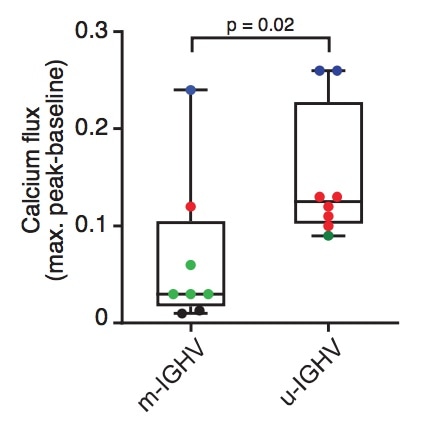
下图显示的是不同钙流水平(对应上面这幅图的颜色)患者的PFS,明显看的出来,钙流水平越低,病程越惰性: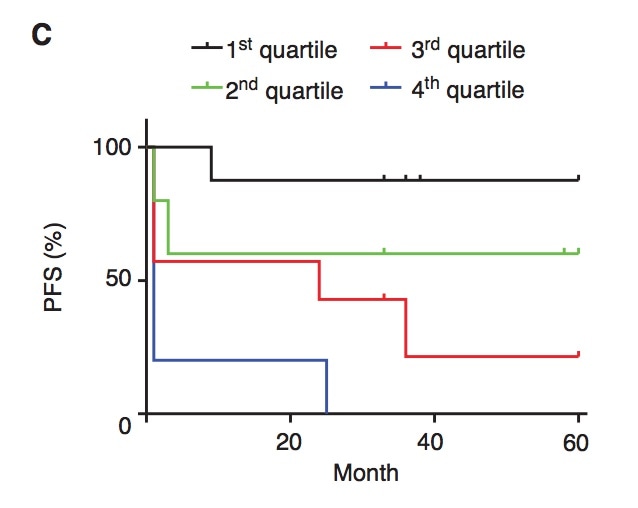
因此,简单地通过IgM刺激BCR受体检测钙内流,可以反映出BCR受体功能,并且与患者预后密切相关。
参考文献:Heitmann JS, Märklin M, Truckenmüller FM, et al. A novel flow cytometry-based assay to measure compromised B cell receptor signaling as a prognostic factor in chronic lymphocytic leukemia [published online ahead of print, 2020 Apr 17]. J Leukoc Biol. 2020;10.1002/JLB.5TA0320-411RR. doi:10.1002/JLB.5TA0320-411RR

