Adaptation and conservation insights from the koala genome
摘要
考拉是唯一仅存的有袋类动物无尾熊科的物种,由于栖息地的减少和大规模的疾病,已经被认定为“濒危动物”。我们对考拉的基因组进行测序,得到了一个完整的和连接的有袋类动物的参考序列,包括着丝粒。我们发现考拉对桉树叶子解毒的能力可能是由于细胞色素 P450 基因家族的扩张,而它的嗅觉、味觉和对植物次生代谢物的适度摄入可能是由于犁鼻器和味觉感受器的扩张。我们鉴定了保护育儿袋中的幼崽的新型哺乳蛋白,并注释了对衣原体疾病反应重要的免疫基因。历史上的人口统计显示,大规模的人口数量流动与澳大利亚巨型动物的减少是同时发生的,而当代人口有生物地理上的局限,并且由于历史上的迁移而增加了近亲繁殖。我们鉴定了具有基因多样性的种群,需要栖息地廊道和建立迁移计划来帮助考拉在野外生存。
结果
基因组景观
考拉有 16 条染色体,其祖先是 2n=14 条染色体,原先的 2 号染色体分裂成为了 4 号染色体和 7 号染色体。有袋类动物的着丝粒比哺乳类动物的着丝粒要小。考拉的着丝粒占考拉单倍体基因组的 2.6 Mb,相当于每条染色体平均有 300kb 的着丝粒物质,和其他具有小着丝粒的物种一样,考拉的着丝粒也缺乏高度排序的卫星阵列。
在新鉴定的重复序列中,有一些与最近在长臂猿着丝粒中描述的复合元素相似,在这些重复序列中,没有高阶卫星阵列,伴随着具有假定着丝粒功能的新复合元素的进化。因此,考拉着丝粒的组成支持了越来越多的证据,即当高度排序的卫星阵列缺失时,可转性元素代表了小着丝粒的主要功能成分。
散布重复序列约占考拉基因组的 47.5%,其中 44% 为转座因子。与其他哺乳动物基因组一样,短散布核元件(SINEs)和长散布核元件(LINEs)是数量最多的核原件(各自在整体元件中占比 35.2% 和 28.9%),而长散布核元件在整个考拉基因组中占比 32.1%。
剧毒耐受能力
考拉吃桉树叶或产生次级代谢物,比如说酚类和萜烯类成分,这类成分对大多数其他的哺乳动物是致命的。
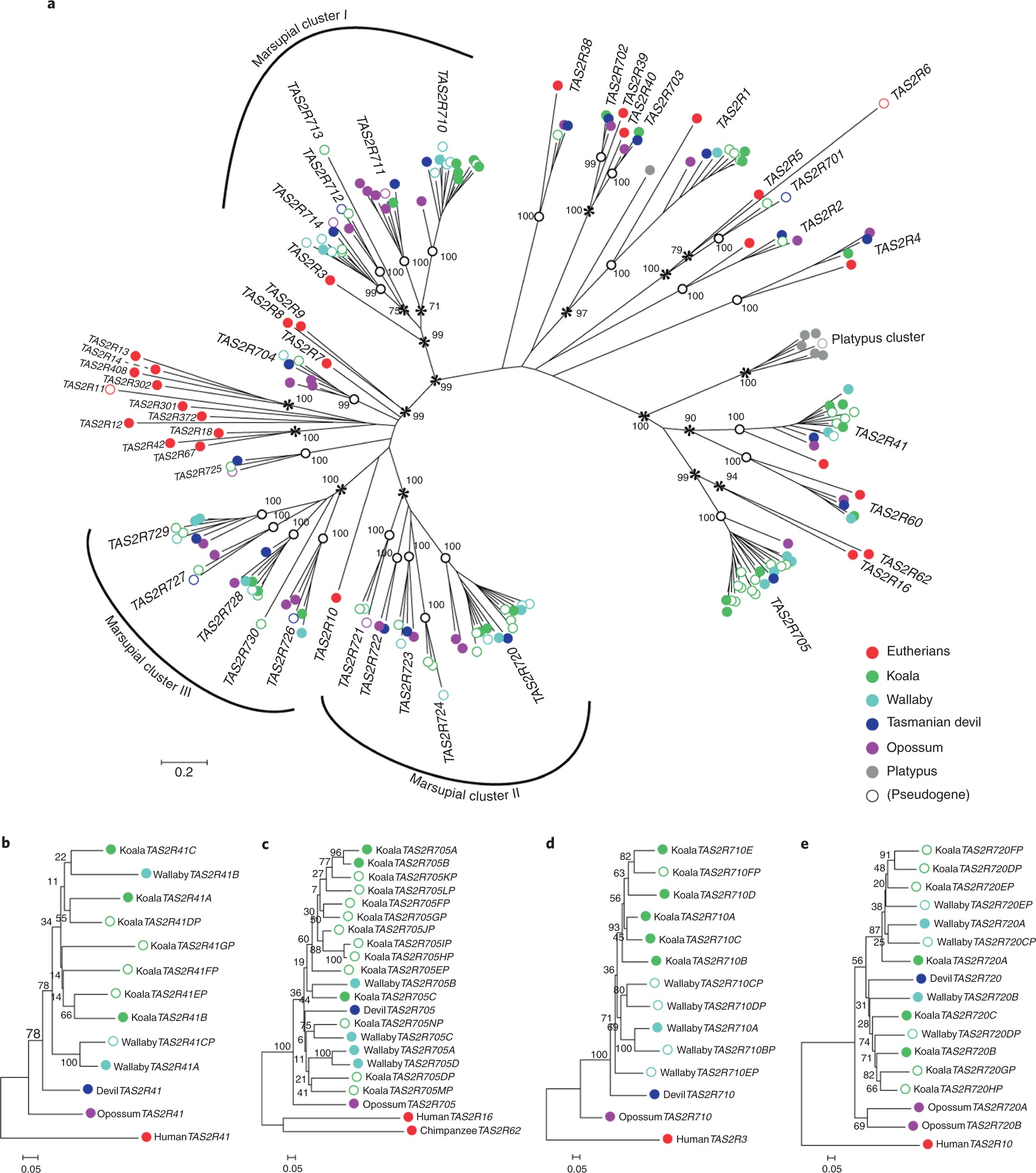
细胞色素 P450 单氧合酶(CYP)基因是一个血红素-硫代酸酶的多基因超家族,该超家族在包括外源性物质在内的一系列化合物的 1 期氧化代谢中发挥解毒作用。这个基因贯穿了整个生命树,存在于植物,动物,真菌,细菌和病毒中。在考拉的基因组中,我们发现了细胞色素 P450 家族的 2 个亚系特异性单系扩展(CYP2Cs)。
通过对来自两只考拉的15个考拉转录组的表达分析,进一步证实了这些 CYP2C 基因的功能重要性,其中 CYP2C 在肝脏中表达特别高,与解毒作用一致。进一步的 CYP 扩增序列分析表明,大多数保守区域处于强纯化选择下,有证据表明,个别的 CYP 密码子经历了偶发的多样化选择,而纯化选择塑造了基因的其余部分。CYP2C 的适应性扩展和重复的维持似乎协同工作,导致较高的解毒酶水平,而纯合和多样化选择之间的相互作用导致 CYPs 内的新功能,这种适应性使考拉能够在富含植物次生代谢物的高度专门化的食物中解毒。
味觉,嗅觉和食物选择
我们发现了一个与非挥发性气味检测相关的 V1R 基因谱系的扩展,与袋獾和灰色短尾负鼠只有一个这样的基因相比,考拉有 6 个这样的基因,而塔马尔沙袋鼠、人类、老鼠、狗、鸭嘴兽和鸡都没有发现这样的基因。一个V1R基因谱系的扩展与考拉区分不同植物次生代谢物的能力是一致的。
令人惊讶的是,考虑到考拉饮食的特化程度,它的嗅觉受体基因(n = 1169)在整个基因库中比灰色短尾负鼠(1431 个基因)、塔马尔沙袋鼠(1660 个基因)和袋獾(1279 个基因)的基因库略小,这可以从考拉的饮食特异性对嗅觉指标的宽松选择中理解。
我们还发现了味道受体家族扩展的基因组证据,这将使考拉能够优化摄入具有更高水分和营养含量的叶子,与有毒植物次生代谢物在其食用植物的浓度一致。树袋熊尝水的能力可能是由于水通道蛋白5 基因明显的功能重复而增强的
TAS2R 家族在识别苦味中起作用,使其能够识别萜类、酚类和糖苷等结构性毒素,这些物质都是桉树的次级代谢物。而考拉相比其他的澳大利亚的的有袋类动物,具有更多的 TAS2R 基因,在哺乳动物中是最多的。
诱导排卵的基因
具有控制雌性排卵的关键基因(LHB、FSHB、ERR1、ERR2),在分娩和射精中起重要作用的前列腺素合成基因(PTGS1、PTGS2、PTGS3)
考拉乳汁的基因组表征
我们发现,有四种哺乳后期蛋白(LLP)基因与 trichosurin 和 β-乳球蛋白紧密相连,这可能使有袋类动物能够在哺乳的各个阶段对乳蛋白组成进行微调,以满足幼崽不断变化的需求。
考拉有袋动物乳汁1 基因(MM1),一个新的有袋动物基因,位于编码非常早期哺乳蛋白(VELP)的基因附近,我们认为,MM1 与位于同一区域的其他三个其他的短且新基因一起,在有袋类动物乳汁中发挥抗菌作用。我们还检测到了另一个抗真菌基因家族——抗菌肽的扩增。
考拉的免疫组和疾病
对参与衣原体疫苗接种试验的 5 只考拉的初步病例/对照关联测试表明,MHCII DMA 和 DMB 基因以及 CD8-a 基因可能参与了对衣原体疫苗的不同免疫应答。
基因组信息保护
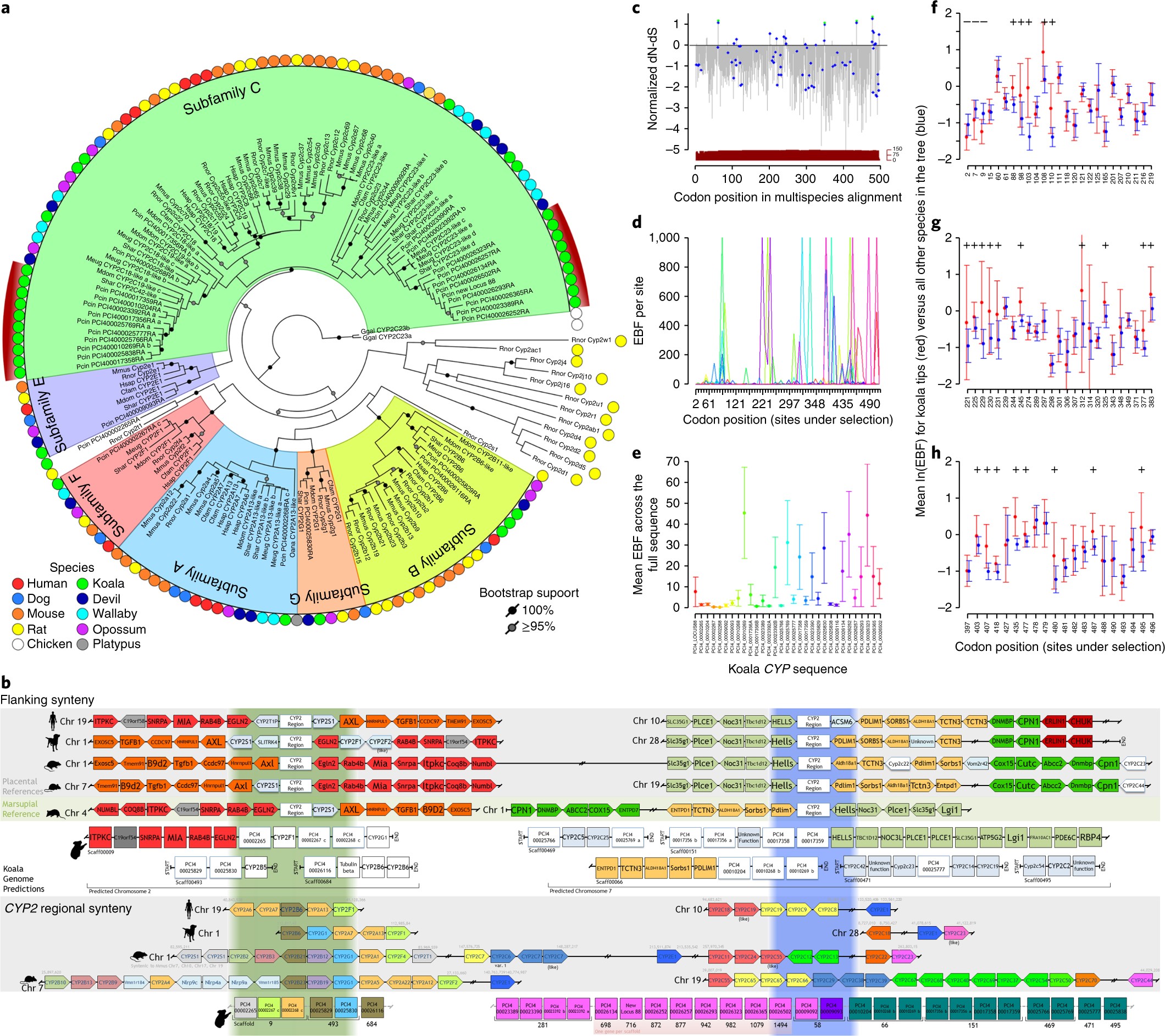
为了推断该物种的历史,我们分析了另外两只考拉的长读参考基因组和短读数据。数据显示,化石记录的现代考拉出现在 35 万年前,这与多种澳大利亚物种迅速减少的化石证据相一致,包括灭绝的巨型动物,包括 5 万年前和 3-4 万年前。考拉也是在这个时期的其中一种动物,只是没有灭绝。
我们利用 1200 个 SNP 位点对最近的考拉样本进行了分析,这些 SNP 位点来自于定位到考拉基因组的目标捕获库。发现显著水平的遗传多样性,伴随有限的细尺度分化一致的长期连接的区域。我们在南部考拉中发现了低基因多样性的证据,这与最近的序列易位的历史相一致。在大陆尺度上,我们展示了与 Brisbane Valley 和 Clarence River 相关的基因流动的生物地理障碍,这是 mtDNA 研究对象所鉴定的,并发现了与 Brisbane Valley 相关的障碍,这在考拉中是不为人所知的,不同地区的近亲繁殖水平各不相同,但受威胁最大的 New South Wales 和 Queensland 显示出高水平的遗传多样性。